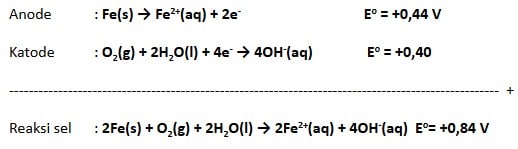Korosi adalah rusaknya benda-benda logam akibat pengaruh lingkungan. Proses korosi juga dijelaskan secara elektrokimia. Contoh korosi pada proses perkaratan besi yang membentuk oksida besi. Proses perkaratan besi tersebut akibat peristiwa teroksidasinya logam besi akibat oksigen.
Lalu apa itu sebenarnya korosi dan penyebabnya?
Untuk mengetahui lebih lengkap tentang korosi, berikut ini akan dijelaskan secara lengkap tentang pengertian korosi, faktor penyebab korosi, cara pencegahan korosi dan contoh soal korosi dengan penjelasannya.
Baca Juga : Fermentasi dan Penjelasannya
Pengertian Korosi
Korosi adalah perubahan atau rusaknya benda-benda logam akibat pengaruh lingkungan yang secara fisika atau kimia terjadi karena hilangnya fungsi mekanis logam tersebut. Besi merupakan salah satu logam yang mudah mengalami korosi atau sering disebut besi berkarat. Besi mengalami korosi jika bersentuhan dengan senyawa asam, air dan mengalami perubahan suhu dalam jangka waktu yang cukup lama dan terus menerus.
Proses terbentuknya korosi merupakan suatu proses elektrokimia. Elektrokimia adalah proses terjadinya reaksi redoks (reduksi oksidasi) secara spontan. Contohnya korosi yang terjadi pada besi akan membentuk oksida besi (Fe2O3.xH2O). Besi akan teroksidasi oleh oksigen di udara dan lama kelamaan akan membentuk korosi. Persamaan yang berlangsung adalah sebagai berikut:
Ion Fe2+ tersebut lalu akan mengalami oksidasi lebih lanjut dengan reaksi dibawah ini.
Baca Juga : Kimia Organik dan Penjelasannya
Faktor Penyebab Korosi
Korosi dapat berlangsung secara cepat ataupun lambat tergantung dari faktor yang mempengaruhinya. Berikut ini beberapa faktor pengaruh terjadinya korosi, anatar lain:
1. Kelembapan udara dan air
Kelembapan udara dan air memiliki pengaruh yang penting pada proses terjadinya korosi. Semakin tinggi kadar uap disekitar logam, maka semakin mudah logam mengalami korosi. Sebaliknya, jika logam berada pada daerah dengan kadar air rendah seperti daerah gurun, maka proses korosi berjalan lebih lambat. Karena itulah untuk memperlambat proses korosi letakkan logam atau besi di tempat yang kering dan tidak lembab.
2. Elektrolit
Elektrolit merupakan tempat atau media yang berfungsi sebagai tempat berlangsungnya transfer muatan yang menyebabkan elektron lebih mudah diikat oksigen di udara. Hal tersebut merupakan salah satu faktor utama terjadinya korosi. Contohnya air hujan bersifat asam dan air laut bersifat asin yang menjadi media yang dapat mempercepat proses korosi. Jadi tidak heran jika besi-besi yang berada di lingkungan pabrik lebih cepat mengalami korosi karena paparan senyawa asam.
3. Terbentuknya sel elektrokimia
Sel elektrokimia terbentuk akibat adanya dua permukaan logam yang saling bersinggungan yang memiliki perbedaan potensial. Logam dengan potensial lebih rendah akan segera melepas elektron ketika bersentuhan dengan logam berpotensial lebih tinggi dan akan mengalami oksidasi oleh oksigen dari udara. Karena hal tersebutlah yang menyebabkan logam dengan potensial rendah lebih cepat mengalami korosi dibandingkan dengan logam dengan potensial lebih tinggi. Contohnya pada paku keling yang terbuat dari tembaga yang digunakan untuk menyambung besi dapat menyebabkan besi disekitar paku keling berkarat lebih cepat.
4. Permukaan logam tidak rata
Permukaan logam yang tidak rata juga menyebabkan terjadinya korosi lebih cepat. Hal tersebut terjadi karena terbentuknya logam-logam kutub muatan di permukaan logamnya. Kutub muatan tersebut berperan sebagai anoda dan katoda.
Baca Juga : Hidrokarbon dan Penjelasannya
Cara Mencegah Korosi
Ada beberapa cara yang dapat dilakukan untuk mencegah terjadinya korosi, antara lain:
- Hindari logam terkena udara luar secara langsung, caranya dengan membuat lingkungan di sekitar logam bebas oksigen, yaitu dengan mengalirkan gas karbondioksida.
- Lakukan pengecatan pada permukaan logam agar tidak bersinggungan langsung dengan udara luar yang mengandung oksigen dan uap air. Hal tersebut dapat memperlambat proses korosi.
- Gunakan elektroplating yaitu melapisi permukaan logam secara elektrokimia. Permukaan logam yang dilapisi berperan sebagai katoda, dan pelapisnya berperan sebagai anoda. Contoh elektroplating seperti pada badan mobil. Badan mobil terbuat dari besi atau baja, untuk mencegah besi atau baja mengalami korosi maka badan mobil dilapisi dengan logam lain yaitu krom yang membuat badan mobil menjadi lebih mengkilap. Proses tersebut merupakan elektroplating.
- Mencegah terbentuknya sel elektrokimia dengan pengorbanan anoda atau perlindungan katoda yaitu dengan cara menyambungkan logam yang akan dilapisi dengan logam yang memiliki potensial elektroda lebih kecil. LOgam tersebut akan berperan sebagai anoda yang nantinya akan mengalami reaksi oksidasi (logam yang terkorosi). Selama logam pelapis atau anoda masih ada, maka logam yang dilapisi katoda tidak akan mengalami korosi.
- Membuat perpaduan dengan cara mencampurkan besi dengan logam lain yang lebih tahan korosi, contohnya seperti nikel dan krom. Campuran ini disebut dengan baja stainless.
Baca Juga : Larutan ELektrolit dan Non Elektrolit Serta Penjelasannya
Contoh Soal Korosi
1. Soal UN 2011 tentang Korosi
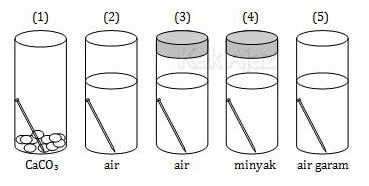
Perhatikan gambar proses korosi berikut!
Proses korosi yang berlangsung paling lambat adalah ….
A. 1
B. 2
C. 3
D. 4
E. 5
Pembahasan
Keterangan masing-masing gambar di atas adalah sebagai berikut:
Paku berada pada tabung terbuka sehingga O2 dapat masuk. Tetapi di dalam tabung terdapat CaCO2 yang bersifat menyerap H2O sehingga udara tetap kering. [lambat korosi]
Paku berada pada tabung terbuka yang berisi air atau paku berada pada medium yang mengandung O2 dan H2O [cepat korosi]
Paku berada pada tabung tertutup yang berisi air. Meskipun tabung tertutup tetapi di dalamnya masih tersisa udara sehingga masih memungkin paku berkarat. [lumayan lambat korosi]
Paku berada pada medium tertutup yang berisi minyak. Berarti jumlah O2 dalam tabung terbatas dan H2O tidak dapat menembus minyak. [sangat lambat korosi]
Paku berada pada tabung terbuka yang berisi air garam. Sedangkan air garam bersifat elektrolit yang dapat mempercepat reaksi oksidasi. [sangat cepat korosi]
Jadi, proses korosi yang berlangsung paling lambat adalah nomor 4 (D).
2. Soal UN 2012 tentang Korosi
Perlindungan korosi yang paling tepat dilakukan untuk melindungi logam pada bagian mesin yang berputar adalah ….
A. mengecat
B. dibuat paduan logam
C. perlindungan katodik
D. melumuri dengan oli
E. dibalut dengan emas
Pembahasan
Bagian mesin yang berputar rentan terjadi gesekan dan cepat aus. Oleh karena itu, perlindungan korosi dengan cara dicat, dibuat paduan logam, perlindungan katodik, apalagi dibalut dengan emas sangatlah tidak efektif.
Perlindungan katodik sangat cocok untuk logam yang digunakan pada bangunan tinggi menjulang, seperti menara atau cerobong asap.
Jadi, perlindungan korosi yang paling tepat pada bagian mesin yang berputar adalah melumuri dengan oli (D).
Baca Juga : Sel Volta dan Penjelasannya
Demikian artikel mengenai Korosi dan Penjelasannya. Semoga artikel ini dapat bermanfaat dan menambah wawasan anda mengenai pelajaran Ilmu Pengetahuan Alam.