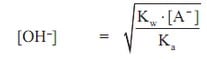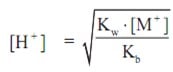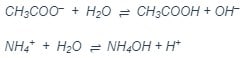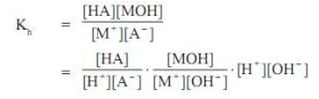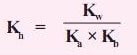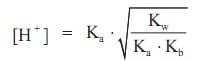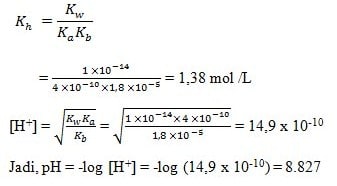Hidrolisis adalah salah satu reaksi sederhana yang paling sering terjadi di kehidupan kita. Reaksi hidrolisis melibatkan molekul air dalam pemecahan senyawa. Contohnya pada manusia, proses hidrolisis terjadi pada proses pencernaan makanan, dimana makanan yang masuk ke sistem pencernaan akan dicerna oleh organ namun diawali dengan hidrolisis dengan molekul air dalam tubuh.
Pada proses penerapan kimia, terdapat banyak proses kimiawi yang terjadi dengan reaksi hidrolisis, hal ini karena hidrolisis banyak digunakan dalam industri untuk melakukan pemecahan struktur kimia tertentu menjadi fraksi atau part yang lebih sederhana. Umumnya senyawa kimia organik memiliki jalur atau pathway masing-masing berbeda untuk setiap senyawa dalam mengalami proses hidrolisis menggunakan air.
Untuk mengetahui lebih lanjut tentang hidrolisis, dibawah ini akan kami jelaskan secara lengkap tentang hidrolisis meliputi pengertian hidrolisis, reakasi-reaksi hidrolisis dan contoh soal hidrolisis.
Baca Juga : Titrasi Asam Basa dan Penjelasan Terlengkap
Pengertian Hidrolisis
Hidrolisis berasal dari bahasa Yunani Kuno yaitu Hidro yang berarti “Air” dan Lisis yang berarti “tidak mengikat”. Setiap reaksi kimia pada hidrolisis dimana molekul air memecah satu atau lebih ikatan kimia. Istilah hidrolisis secara luas digunakan untuk reaksi substitusi, eliminasi dan solvaso dimana air adalah nukleofil.
Hidrolisis adalah jenis reaksi dekomposisi suatu zat dengan menggunakan air sebagai media pemecah ikatan zat tersebut.
Hidrolisis merupakan kebalikan dari reaksi sintetis kondensasi yang merupakan proses dua molekul saling bergabung membentuk molekul yang lebih kompleks dengan melepas air. Cara membedakan dua molekul tersebut sangat mudah, reaksi hidrolisis membutuhkan air sedangkan reaksi kondensasi menghasilkan air. Air atau H2O mengalami fragmentasi menjadi ion hidrogen (H+) dan ion hidroksida (OH-) yang berperan dalam reaksi hidrolisis.
Terdapat juga beberapa pendapat dari beberapa alhi yang mengemukakan pendapatnya tentang hidrolisis. Dibawah ini merupakan pendapat menurut ahli tentang hidrolisis, antara lain:
Menurut Biology LibreTexts, Hidrolisis adalah reaksi yang menghasilkan pemecahan polimer menjadi monomer dengan menggunakan molekul air dan katalis enzimatik. Dalam reaksi hidrolisis, air digunakan untuk memecah polimer menjadi monomer dan merupakan kebalikan dari proses sintetis dehidrasi yang membentuk air saat mensintesis plomer dari monomer.
Menurut Encyclopedia Britannica, dalam kimia dan fisiologi, hidrolisis adalah reaksi dekomposisi ganda dengan air sebagai salah satu rektan.
Baca Juga : Hidrokarbon dan Penjelasannya
Jenis Jenis Hidrolisis
Reaksi hidrolisis berlangsung dengan beberapa bahan kimia awal dan reaktan. Berdasarkan jenis reaktan awal, hidrolisis memiliki banyak jenis. Namun berikut ini akan kami jelaskan jenis hidrolisis garam saja, karena hidrolisis garam merupakan jenis yang paling banyak di terapkan dalam kimia. Berikut penjelasannya.
Garam Parsial (Asam Lemah-Basa Kuat)
Hidrolisis parsial terjadi akibat garam yang terbentuk dari reaksi asam lemah dan basa kuat yang dilarutkan dalam air, maka menyebabkan kation dari basa tidak bisa terhidrolis, sedangkan anion asam kuat akan mengalami proses hidrolisis.
Disebut hidrolisis parsial karena tidak semua bagian terhidrolisis. Berikut ini rumus yang digunakan untuk perhitungan garam parsisal, antara lain:
Berdasarkan reaksi tersbeut, larutan garam memiliki kandungan ion natrium dan ion asetat. Ion natrium bertindak sebagai asam konjugasi dari basa kuat dan tidak memiliki pengaruh terhadap keasaman larutan.Sedangkan ion asetat bertindak sebagai basa konjugasi dari asam lemah yang berreaksi dengan air dan meningkatkan pH larutan menjadi basa.
Konstanta kesetimbangan reaksi tersebut adalah konstanta ionisasi Kb untuk basa CH3COO–. Nilah Kb dapat dihitung berdasarkan nilai konstanta ionisasi air (Kw) dan Ka.
Rumus ion asetat dan asam konjugasi:
Rumus menentukan pH dari Hidrolisis:
Baca Juga : Kimia Organik dan Penjelasannya
Garam Parsial (Asam Kuat-Basa Lemah)
Hidrolisis tersebut terjadi ketika garam yang berasal dari asam kuat dan basa lemah dilarutkan dalam air. Contohnya ketika garam ammonium klorida (NH4Cl) terbentuk dari reaksi basa lemah ammonia dengan asam kuat HCl:
Larutan mengandung ion ammonium (NH4+) dan ion klorida (Cl–). Ion klorida tidak memiliki pengaruh terhadap keasaman larutan meskipun HCI merupakan asam kuat. Sedangan ion ammonium adalah asam konjugasi dari amonia bereaksi dengan air sehingga membentuk ion hidronium (H3O+) yang memberikan suasana asam pada larutan.
Konstanta kesetimbangan pada reaksi tersebut sama dengan konstanta ionisasi disebut Ka untuk asam NH4+.
Untuk menentukan nilai Ka digunakan dengan menggunakan konstanta ionisasi (Kw) dan merupakan konstanta ionisasi dari basa konjugasi NH3.
Rumus yang digunakan untuk menghitung pH akhir dari larutan hidrolisis, antara lain:
Baca Juga : Fermentasi dan Penjelasannya
Garam Total (Asam Lemah-Basa Lemah)
Pada hidrolis jenis ini, garam yang dihasilkan dari reaksi asam lemah dan basa lemah ketika dilarutkan dalam air akan terhadi hidrolisis total. Hal ini karena ion positif dari basa lemah dan ion negatif dari basa memungkinkan terjadinya hidrolisis.
Contohnya reaksi antara asam asetat yang merupakan asam lemah dengan amonium hidrosida yang merupakan basa lemah akan menghasilkan garam amonium asetat dan melepas air.
Di dalam air, baik anion CH3COO– maupun kation NH4+ dari amonium asetat dapat terhidrolisis dengan masing-masing menghasilkan asam dan basa:
Konstanta kesetimbangan atau tetapan hidrolisis dalam reaski tersebut adalah Kh yang berbeda dengan hidrolisis sebagaian. RUmus yang berlaku yaitu:
Maka
Rumus yang digunakan untuk menentukan pH dari larutan hidrolisis total adalah:
Baca Juga : Larutan Penyangga dan Penjelasannya
Contoh Soal Hidrolisis
Ph larutan garam NH4CN adalah 0,2M. Diketahui Ka HCN = 4,0 x 10-10 mol/L, Kb NH3 = 1,8 x 10-5 mol/L adalah:
Penyelesaian:
Baca Juga : Ikatan Kimia dan Penjelasannya
Demikian artikel mengenai Hidrolisis dan Penjelasannya. Semoga artikel ini dapat bermanfaat dan menambah wawasan anda mengenai pelajaran Ilmu Pengetahuan Alam.