Titrasi merupakan langkah yang digunakan untuk menentukan kadar suatu larutan. Dalam titrasi, larutan yang volumenya terukur akan direaksikan dengan larutan lain yang diketahui kadarnya (larutan standar) secara bertahap. Berdasarkan jenis reaksi yang terjadi, titrasi dibedakan menjadi 3 kelompok, yaitu titrasi asam basa, titrasi pengendapan, dan titrasi redoks.
Titrasi asam basa merupakan metode yang paling banyak di gunakan untuk menentukan kadar suatu larutan. Karena itulah kali ini kita akan membahas secara lengkap tentang titrasi asam basa, meliputi pengertian titrasi asam basa, cara kerja titrasi, rumus hitung dan contoh soal titrasi asam basa dengan penjelasannya.
Reaksi asam dan basa membantuk suatu garam dan air yang menjadi salah satu ciri reaksi kimia yang umum di laboratorium. Hal ini karena terdapat banyak senyawa yang bertindak dan memiliki sifat asam atau basa tersebut. Akibatnya prinsip reaksi penetralan dari asam basa tersebut paling banyak diterapkan dalam penentuan kadar suatu zat yang tidak diketahui melalui titrasi asam basa. Lebih lengkapnya, simak penjelasan dibawah ini tetang titrasi asam basa.
Baca Juga : Polimer dan Penjelasan Terlengkap
Pengertian Titrasi Asam Basa
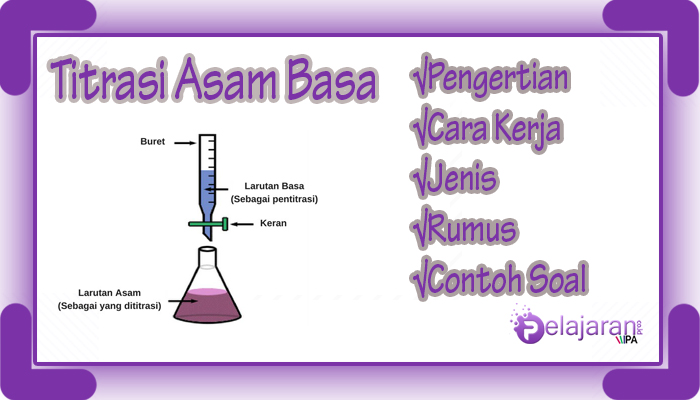
Titrasi adalah prosedur yang digunakan dalam kimia untuk mementukan konsentrasi kadar suatu zat yang tanpa diketahui dengan menggunakan zat yang telah diketahui kadarnya. Pada titrasi asam basa prinsip yang digunakan yaitu zat yang bersifat asam akan di titrasi dengan larutan basa yang telah diketahui kadarnya atau sebaliknya zat yang bersifat basa akan dititrasi dengan larutan asam yang telah diketahui kadanya.
Prinsip titrasi asam basa menerapkan prinsip reaksi asam basa dimana ketika suatu asam dan basa dicampurkan atau direaksikan maka terjadi reaksi penetralan yang menghasilkan suatu gram dan air dengan pH yang netral.
Baca Juga : Tata Nama Senyawa Hidrokarbon dan Penjelasannya
Istilah pada Titrasi Asam Basa
Dalam titrasi asam basa terdapat beberapa istilah yang perlu diketahui. Berikut ini beberapa istilah yang digunakan, antara lain:
- Titik akhir titrasi yaitu titik saat indikator asam basa mengalami perubahan warna
- Titik ekuivalen yaitu titik ketika asam basa tepat habis bereaksi
- Pentiter yaitu zat yang menitrasi asam basa yang ingin ditentukan kemolarannya
- Daerah perubahan pH drastis yaitu daerah saat terjadinya sedikit penambahan tetes pentiter yang akan mengubah warna indikator asam basa.
Baca Juga : Radiasi Benda Hitam dan Penjelasannya
Cara Kerja Titrasi Asam Basa
Untuk menentukan zat yang tidak diketahui kadarnya, langkah pertama yang dilakukan adalah dengan mengetahui sifat zat tersebut, apakah bersifat asam atau basa dengan cara mengukur pHnya.
Saat zat tersebut telah di ketahui, selanjutnya tentukan larutan apa yang digunakan untuk menitrasi zat tersebut, apakah asam atau basa. Dalam titrasi, zat yang diuji akan ditambah larutan yang telah diketahui kadarnya secara perlahan hingga terjadi reaksi penetralan.
Ketika pH pada larutan campuran tersebut netral, maka menandakan bahwa seluruh zat sampel telah bereaksi dengan larutan yang digunakan untuk menitrasi. Cara mengetahui pH larutan tersebut yaitu dengan menggunakan pH meter, namun dalam titrasi cara umum yaitu dengan menggunakan indikator.
Baca Juga : Hidrokarbon dan Penjelasannya
Jenis Titrasi Asam Basa
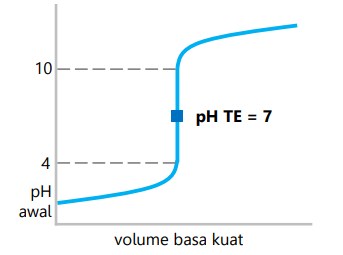
Titrasi asam kuat dengan basa kuat
- Zat pentiter adalah basa kuat.
- Daerah perubahan pH drastis 4 – 10.
- pH titik ekuivalen 7.
- Indikator yang dapat digunakan adalah metil merah, bromtimol biru, dan fenolftalein (lebih tajam).
- Contoh: HCl dengan NaOH.
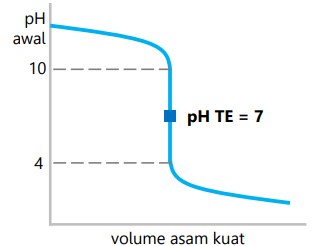
Titrasi basa kuat dengan asam kuat
- Zat pentiter adalah asam kuat.
- Daerah perubahan pH drastis 4 – 10.
- pH titik ekuivalen 7.
- Indikator yang dapat digunakan adalah metil merah, bromtimol biru, dan fenolftalein (lebih tajam).
- Contoh: NaOH dengan HCl.
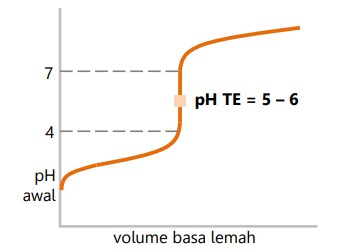
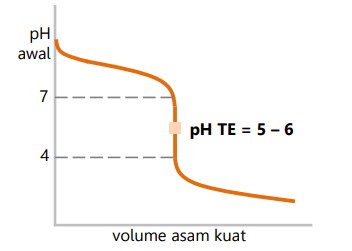
Titrasi asam kuat dengan basa lemah
- Zat pentiter adalah basa lemah.
- Daerah perubahan pH drastis 4 – 7.
- pH titik ekuivalen 5 – 6.
- Indikator yang dapat digunakan adalah metil merah.
- Contoh: HCl dengan NH4OH.
Titrasi basa lemah dengan asam kuat
- Zat pentiter adalah asam kuat.
- Daerah perubahan pH drastis 4 – 7.
- pH titik ekuivalen 5 – 6.
- Indikator yang dapat digunakan adalah metil merah.
- Contoh: NH4OH dengan HCl.
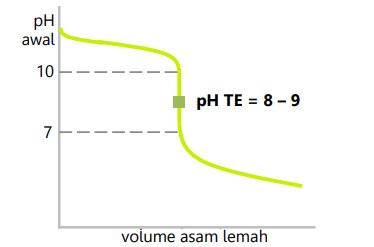
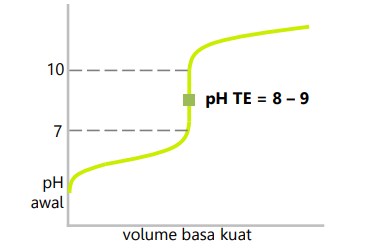
Titrasi basa kuat dengan asam lemah
- Zat pentiter adalah asam lemah.
- Daerah perubahan pH drastis 7 – 10.
- pH titik ekuivalen 8 – 9.
- Indikator yang dapat digunakan adalah fenolftalein.
- Contoh: NaOH dengan CH3COOH.
Titrasi asam lemah dengan basa kuat
- Zat pentiter adalah basa kuat.
- Daerah perubahan pH drastis 7 – 10.
- pH titik ekuivalen 8 – 9.
- Indikator yang dapat digunakan adalah fenolftalein.
- Contoh: CH3COOH dengan NaOH.
Titrasi asam lemah dengan basa lemah atau sebaliknya tidak dilakukan karena beberapa alasan, antara lain:
- Perubahan drastis pH terjadi sangat singkat
- Tidak terdapat indikator yang cukup teliti untuk mengamati perubahan
- Reaksi berlangsung lambat dan tidak tuntas
Baca Juga : Kimia Organik dan Penjelasannya
Rumus Titrasi
Cara perhitungan pada titrasi yaitu berdasarkan jumlah mol masing-masing zat yang bereaksi dalam satu titrasi. Prinsip tersebut yaitu dalam satu reaksi yang telah seleai, jumlah dari reaktan yang digunakan sama dengan jumlah rektan lain yang bereaksi, maka pada titrasi asam basa hal tersebut dapat ditulis sebagai mol asam dan mol basa, atau
Mol asam = Mol basa.
Mol ditentukan dari konsentrasi dan volume, atau
Mol = Konsentrasi x Volumer
Dapat disimpulkan dari persamaan tersebut yaitu:
(Konsentrasi x Volume) asam = (Konsentrasi x Volume) basa
Yang dirumuskan sebagai berikut:
Ma x Va = Mb x Vb
Senyawa yang memiliki valensi lebih dari 1, dirumuskan sebagai berikut:
Ma x Va x na = Mb x Vb x nb
Keterangan:
Ma adalah konsentrasi asam,
Va adalah volume asam,
na adalah jumlah valensi asam,
Mb adalah konsentrasi basa,
Vb adalah volume basa,
nb adalah jumlah valensi basa.
Baca Juga : Fermentasi dan Penjelasannya
Contoh Soal Titrasi Asam Basa
Soal 1 : Sebanyak 5 mL larutan HCl yang tidak diketahui konsentrasinya dititrasi dengan NaOH 1 M. Pada titrasi dibutuhkan 10 mL NaOH sehingga indikator PP berubah warna menjadi merah muda. Tentukan konsentrasi HCl.
Penyelesaian:
Ma x Va = Mb x Vb
Ma x 5mL = 1M x 10mL
Ma = 2M
Jadi, konsentrasi HCl adalah 2M
Soal 2: Tentukan jumlah larutan HCl 0.105M yang digunakan untuk menitrasi 22.5 mL larutan NH3118M
Penyelesaian:
HCl + NH3 NH4Cl , maka valensi = 1
Ma x Va = Mb x Vb
0.105M x Va = 0.118M x 22.5mL
Va = 25.3 mL
Baca Juga : Larutan Penyangga dan Penjelasannya
Demikian artikel mengenai Titrasi Asam Basa dan Penjelasan Terlengkap. Semoga artikel ini dapat bermanfaat dan menambah wawasan anda mengenai pelajaran Ilmu Pengetahuan Alam.