Benzena adalah salah satu bahan kimia yang banyak digunakan dalam industri kimia. Benzena termasuk golongan senyawa hidrokarbon aromatik. Contohnya penggunaan kapur barus yang biasa di gunakan pada lemari. Kapur barus mengeluarkan bau wangi yang dihasilkan dari senyawa yang mengandung aromatik. Aromatik tersebut merupakan senyawa turunan benzena. Lalu apa itu benzena?
Untuk mengetahui lebih lanjut tentang benzena dan turunannya, berikut ini akan dijelaskan lebih lanjut tentang benda dan turunannya, meliputi pengertian, senyawa turunan, reaksi dan contonya lengkap dengan penjelasannya.
Baca Juga : Larutan Penyangga dan Penjelasannya
Pengertian Benzena
Benzena adalah senyawa organik dengan rumus molekul C6H6 yang tersusun atas 6 buah atom karbon gabungan yang membentuk sebuah cincin dengan satu atom hidrogen yang terikat pada masing-masing dari atom dan hidrogen.
Benzena termasuk golongan senyawa hidrokarbon aromatik. Aromatik merupakan istilah yang berkaitan dengan struktur dan sifat-sifat khas tertentu kecuali dengan aromanya. Hal ini karena senyawa-senyawa aromatik tidak berbau.
Benzena memiliki satu atom H yang terikat di setiap atom C dan memiliki total 3 buah ikatan rangkap dua yang berselang seling.
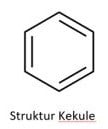
Ada dua jenis cara menggambat struktur benzena, yaitu struktur kekule dan struktur delokalisasi π.
Struktur kekule ditemukan pada tahun 1865 oleh Kekule. Struktur kekule menyatakan bahwa 6 atom karbon benzena terletak pada sudut sudut yang membentuk heksagon beraturan dengan satu atom hidrogen yang mengikat pada setiap atom karbon dengan ikatan tunggal dan ikatan ganda berseling.
Sedangkan pada struktur delokalisasi π, ikatan rangkap benzena digambarkan sebagai lingkaran yang menyatakan terjadinya delokalisasi ikatan π. Deokalisasi terjadi karena elektron pada ikatan rangkap yang berseling tersebar di seluruh cincin.
Baca Juga : Fermentasi dan Penjelasannya
Senyawa Turunan Benzena
Senyawa turunan benzena memiliki turunan senyawa yang terbagi menjadi tiga jenis golongan, yaitu benzena monosubstitusi, benzena disubstitusi, dan benzena substitusi lebih dari dua.
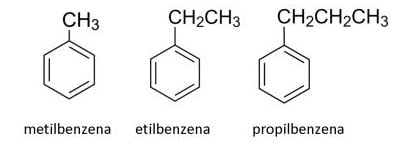
Benzena monosubstitusi adalah benzena dengan satu substituen yang menggantikan salah satu atom H. Benzena monosubstitusi memiliki tata nama “nama substituen + benzena”.
Perhatikan contoh dibawah ini:
Berikut ini beberapa nama substituen yang terdapat pada senyawa benzena, antara lain:
[table id=26 /]
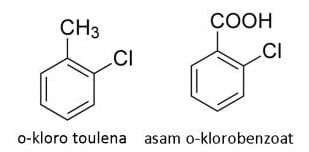
Benzena disubtitusi memiliki dua substituen sehingga terjadi isomer posisi. Cara membedakan isomoer posisi pada benzena disubstusi, yaitu digunakan penamaan orto (o), meta (m), para (p).
Orto digunakan jika substituen berada pada atom C nomor 1 dan 2. Meta digunakan jika substituen berada pada atom C nomor 1 dan 3, sedangkan para digunakan jika substituen berada pada atom C nomor 1 dan 4.
Penomoran tersebut memperhatikan substituen terdekat sheingga tidak ada 1 dan 5 melainkan pada nomor 1 dan 3. Lebih jelasnya, perhatikan contoh dibawah ini:
Lalu bagaimana jika substituennya berbeda? Jika substituen berbeda, maka salah satu substituennya menjadi senyawa utama sedang lainnya menjadi cabangnya.
Cara pemilihan senyawa utama memperhatikan aturan dibawah ini, jika senyawa yang lebih diprioritaskan menjadi senyawa utama.
(lebih prioritas) –COOH, –SO3, –CH3, –CN, –OH, –NH2, –R, –NO2, –X
Berikut nama-nama senyawa dengan substituen tersebut, antara lain:
[table id=27 /]
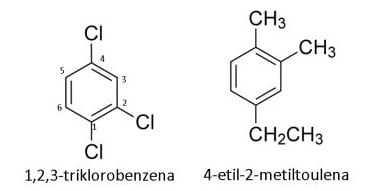
Lalu, bagaimana jika terdapat lebih dari dua substituen? Cara penamaannya hampir sama. Untuk senyawa dengan substituen yang sama , maka diberi nomor dengan substituen terdekat menjadi 1, lalu digunakan penamaan seperti senyawa organik pada umumnya.
Sedangkan untuk substituen yang beda, salah satu substituennya menjadi senyawa utama. Lebih jelasnya perhatikan contoh dibawah ini:
Sifat Bezena
- Benzena termasuk senyawa beracun yang bersifat karsinogenik (dapat menyebabkan kanker).
- Benzena berwujud cair suhu ruang, tidak berwarna, dan mudah menguap
- Memiliki titik leleh 6°C dan titik didih 80°C
- Benzena bersifat nonpolar.
- Benzena larut dalam pelarut kurang polar dan nonpolar seperti eter dan tetraklorometana.
- Benzena tidak larut dalam pelarut polar seperti air
- Benzena tidak reaktif tapi mudah terbakar.
Baca Juga : Kimia Organik dan Penjelasannya
Reaksi Benzena
Benzena cenderung mudah mengalami reaksi substitisi jika dibandingkan dengan reaksi adisi. Reaksi substiyusi benzena melibatkan serangan pereaksi bermuatan positif parsial atau utuh yang suka elektron (elektrofil) pada cincin benzena. Karena itulah, reaksi substitusi benzena sering disebut reaksi substitusi elektrofilik. Berikut ini reaksi-reaksi substitusi pada benzena, antara lain:
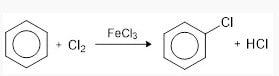
Halogenasi
Benzena bereaksi dengan halogen seperti Cl2 dan Br2 dan bantuan katalis besi(III) halida (FeCl3 atau FeBr3) membentuk senyawa halobenzena.
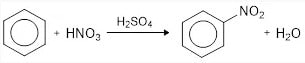
Nitrasi
Benzena bereaksi dengan asam nitrat pekat dengan katalis asam sulfat pekat membentuk nitrobenzena.
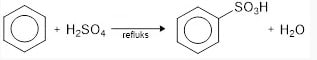
Sulfonasi
Benzena bereaksi dengan SO3 dalam asam sulfat pekat jika dipanaskan membentuk asam benzenasulfonat.
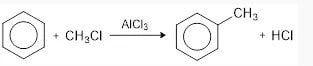
Alkilasi Friedel-Crafts
Benzena bereaksi dengan alkil halida dan bantuan katalis aluminium klorida (AlCl3) membentuk alkilbenzena.
Baca Juga : Hidrokarbon dan Penjelasannya
Contoh dan Kegunaan Benzena
Sebenarnya contoh benzena dapat dengan mudah ditemukan dalam kehidupan sehari-hari, hanya saja kita sering tidak sadar dan tidak paham dengan senyawa-senyawa benzema. Untuk itu, berikut ini beberapa contoh senyawa benzena dan turunanya yang sering ditemukan dalam kehidupan sehari-hari.
- Asam benzoat, merupakan bahan baku pembuatan sakarin, dan aspirin.
- Asam salisilat, digunakan pada obat kutil, jerawat, dan ketombe
- Natrium benzoat, sebagai pengawet makanan
- Nitrobenzena, digunakan pada pewangi pada semir sepatu
- Metil salisilat, digunakan pada balsam
- Parasetamol, sebagai obat penurun panas
- Vanilin, sebagai perisa dan aroma vanila
Baca Juga : Unsur Unsur Radioaktif dan Penjelasannya
Demikian artikel mengenai Benzena dan turunannya serta Penjelasannya. Semoga artikel ini dapat bermanfaat dan menambah wawasan anda mengenai pelajaran Ilmu Pengetahuan Alam.